| 바이오 분야에 따른 3D 바이오프린터의 활용성 | |
|---|---|
| Date 2022-09-26 13:49:26 |
|

(주) 로킷헬스케어
yeonho.kim@rokit.co.kr
1. 3D 바이오 프린터
Charles W. Hull은 1986년에 최초로 소재를 층층이 쌓아 올리면서 3 차원 프린팅이라는 3D 프린팅의 개념을 발표하였다.
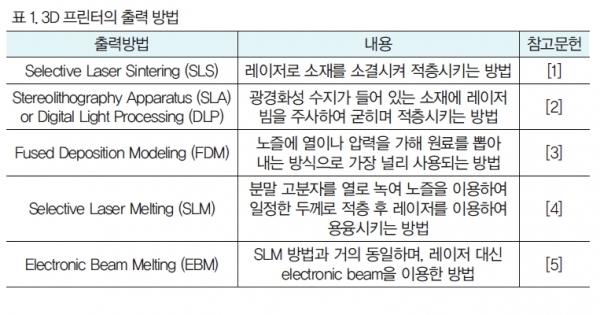
(3D bioprinting of tissues and organs; Material incress manufacturing by rapid prototyping techniques). 3D 프린팅의 원리는 주로 열을 사용하여 녹는점이 높은 물질을 녹여서 프린팅 후, 굳히는 원리를 사용하고 있다. 3D 프린터 제품마다 출력의 방법이 다양하게 있는데, 대표적인 방법들은 표 1 과 같다. 이러한 방법을 활용하여, 현재 3D 프린팅은 산업에서 빠르고 정확하게 시제품을 생산할 수 있고, 가정에서 손쉽게 제품 창작활동과 학교에서 교육에 활용되기도 한다. 하지만, 최근 생분해성 고분자의 연구가 활발히 진행되면서, 녹는점이 낮은 생분해성 고분자의 3D 프린팅의 수요가 높아지고 있다.
3D 바이오 프린터는 생분해성 고분자를 출력하여, 바이오 분야에서 각광받고 있는 기술이다.
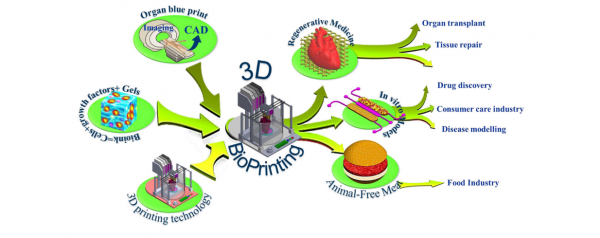
기본적인 원리로 열을 사용하는 3D 프린터와 달리, 3D 바이오 프린터는 공압으로 출력하는 방식을 사용하여 열에 변성이 가능한 생분해성 고분자를 안정하게 출력할 수 있다. 생분해성 고분자는 하이드로겔 형태로 친환경, 친세포성과 낮은 독성, 값싼 원료가 장점이며, 대표적인 예로 젤라틴, 알지네이트와 한천이 있다. 이 기술은 의학, 약학, 식품학 등 다양한 바이오 분야에서 응용되고 있으며, 앞으로도 많은 영역에서 기술의 발전이 기대된다. (그림 1)
2. 의학 분야에서의 3D 바이오 프린터
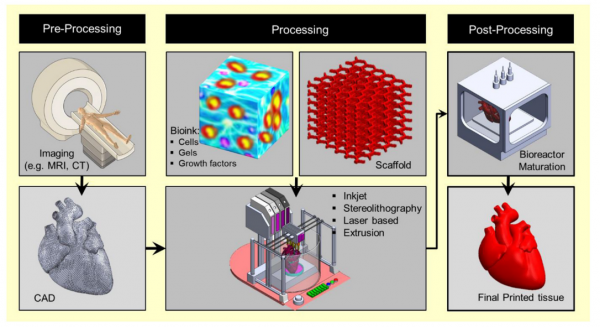
3D 바이오 프린터가 가장 많이 활용되고 있는 분야는 바로 의학 분야이다. 치과에서는 생체 소재를 활용하여 기존의 치기공사가 제작하던 레진을 3D 바이오 프린터가 제작한다. 뿐만 아니라 재생의학 분야에서 3D 바이오 프린팅으로 장기를 재생시키려는 많은 연구가 진행되고 있다. 재생의학에서의 3D 바이오 프린팅의 가장 핵심 기술은 기존 2D 형태의 세포 배양에서 3D 형태의 세포 배양으로의 전환이다. 기존의 세포 배양은 모두 Petri-dish에서 세포를 배양하면, 세포들이 Petri-dish 바닥에 붙어서 2D 형태로 배양되었다. 하지만 세포를 적절한 바이오 잉크에 고루 분산시킨 후 큐브 형태 등 적절한 형태로 3D 프린팅 후에 배지에 침지시켜 배양시키게 되면 3차원 형태로 세포가 자라게 된다 (그림 2). 이 기술은 세포에서 조직의 형태까지 배양시킬 수 있다. 조직재생을 위해서는 줄기세포와 생체소재에 대한 연구가 요구된다. 줄기세포가 잘 성장할 수 있는 성장요인과 사이토카인 등의 조건 확립이 필요하다. 생체소재는 대부분 수용성 물질로 이루어져 있지만, 배양액에 침지되어 줄기세포가 조직이 될 때까지 지지층의 역할을 수행해야한다. 뿐만 아니라 세포와의 반응성과 독성이 없어야 한다. 환자에게 필요한 조직을 MRI와 CT로 스캔한 후 조직의 크기와 형태를 프로그램화 시킨다. 그 후 환자의 세포 혹은 줄기세포와 바이오 잉크를 혼합하여 프린팅 후 배양기에서 배양시켜 원하는 조직으로 키워 이식하는 과정이다.
현재 3D 바이오 프린팅을 활용한 재생의학에서 가장 많이 실현되고 있는 분야는 피부조직 재생이다. Leila의 연구에 따르면, Adipose-
derived stem cell을 포함하고 있는 바이오 잉크를 3D 바이오 프린팅하여 화상을 입은 쥐에게 바이오 잉크를 부착시켰을 때, Adipose-
derived stem cell은 성장하여 21일 안에 완전히 상피세포의 재생됨을 확인하였다 [7]. 현재 재생의학에서는 3D 바이오 프린터로 만들어진 패치의 형태로 환부에 붙여 조직을 재생시키는 방법을 사용하고 있다. 하지만 3D 바이오 프린터를 활용한 재생의학의 최종 목적은
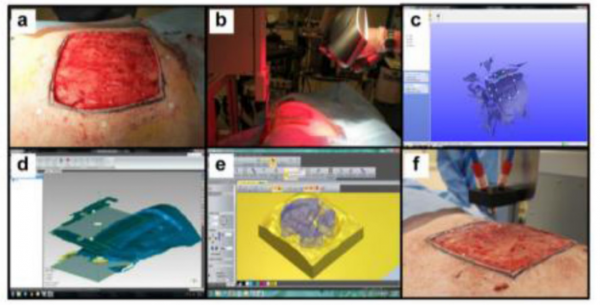
In situ 바이오 프린팅이다. In situ 바이오 프린팅은 환부에 직접 3D 바이오 프린터가 바이오 잉크를 출력하여 조직을 재생시키는 기술이다. 이 기술을 실현하기 위해서는 3D 차원의 환부를 오차 없이 실시간 scan 능력과 생물의 호흡으로 인한 움직임 까지 모두 계산해야한다는 허들이 있다. In situ 바이오 프린팅의 사례로 돼지 피부의 환부를 실시간 스캔하고, 프로그램화시켜 환부에 직접 바이오 프린트하여 피부가 재생되는 결과를 발표하였다 (그림 3). 이 결과를 바탕으로 3D 바이오 프린터가 의료 수술의 대체성의 비전을 보여주었다.
그림 3. 돼지 피부 환부에 3D 바이오 프린터를 활용한 피부재생 기술 [8].
3. 약학 분야에서의 3D 바이오 프린터
약학 분야에서의 3D 바이오 프린터는 신약, 건강기능식품 개발 과정에서 활용될 수 있다. 개발 과정 중 임상시험 전 In vitro 약물 효능 및 독성학적 평가에 새로운 지평이 열릴 것으로 기대하고 있다. 앞서 설명했듯이, In vitro 실험에서의 2D 세포 실험을 3D 세포실험의 전환은 약물의 효능과 독성 평가를 보다 체내 조건과 동일하게 설정할 수 있다. 기존의 2D 형태의 약물 효능과 독성 평가는 세포와 약물의 표면적이 제한적이기 때문에 In vitro 결과와 In vivo, 임상시험 결과가 큰 차이가 있었다. 2D 세포 실험은 세포가 바닥에 붙어 있는 형태이기 때문에 약물이 세포의 단표면에만 노출이 되어, 체내와 같은 3D 형태에서 약물이 세포에 모든 표면에 작용하는 것과는 차이가 발생할 수밖에 없다. 또한 기존 In vitro 실험은 복합적 요소 조건 (세포의 종류, 성장 요인, 영양소 등)을 설정함에 한계가 있다. 한 가지 예로 기존 실험법으로 Cell-Cell 간의 약물 효과를 평가할 수 있지만, Cell-matrix, Cell-tissue, Cell-organ 등 더 복잡한 조건에서의 약물 효과를 평가할 수 없다. 따라서 기존 연구자들 사이에서도 In vitro 실험 결과의 신뢰성을 많이 얻기 어려웠다. 3D 바이오 프린터를 활용한 세포와 바이오 잉크의 출력은 약물의 작용을 3D 형태로 노출 시킬 수 있으며, 더 나아가서 인공 장기를 재생시켜 실제 장기 내 약물 작용을 시뮬레이션할 수 있다.
약학 분야에서는 3D 바이오 프린터로 제제연구의 편의성에 기여하고 있다. 약학 분야에서 최근 하이드로겔 패치와 구강붕해필름의 관심도가 높아지고 있는데, 두 제형은 타 제형과 다르게 lab-scale 제품과 scale-up 제품에서의 품질 차이가 굉장히 크다. 그 대표적인 이슈로 두 제형은 유독 많은 종류의 고분자를 섞어야하는 제형 특성을 가지고 있기 때문에 안정성과 재현성에서 차이가 크게 난다. 또한, 제품 두께가 제품의 품질과 약물의 함량을 결정짓기 때문에 lab-scale에서 품질관리가 상당히 어려운 문제가 있다. 이러한 문제점을 해결하기 위해, 3D 바이오 프린터를 도입하는 추세이며, 많은 연구에서 활용되고 있다. 한 연구에서는 3D 바이오 프린터를 이용하여 PEGylated liposomal
doxorubicin 약물을 젤라틴과 CMC 혼합 바이오 잉크에 교반하여 하이드로겔 패치 제형을 출력 및 평가에 성공하였다 (그림 5A) [10]. 또한 일본에서는 3D 바이오 프린터를 활용하여 카테킨을 함유한 Hydroxypropyl Methylcellulose 기반의 구강붕해필름을 제작한 사례를 발표하였다 (그림 5B) [11]. 이러한 연구는 추후 3D 바이오 프린터가 약학 분야의 발전에 기여할 것으로 사료된다.
그림 5. 3D 바이오 프린터를 이용한 하이드로겔 패치 (A)와 구강붕해필름 (B)의 개발 [10,11].
4. 식품 분야에서의 3D 바이오 프린터
3D 바이오 프린터의 기술로 큰 흐름이 바뀔 영역이 식품분야로 사료된다. 지금까지 식품분야는 바이오 분야에서 기술의 진보성이 가장 느렸던 분야였다. 하지만 3D 바이오 프린터의 활용은 기존의 패러다임을 바꿀 초석으로 기대하고 있다. 최근 이상기온, 미세플라스틱 등 환경에 대한 인류의 관심이 높아지고 있다. 3D 바이오 프린터는 식품의 환경문제 해결의 초석 기술이 될 수 있다. 그 기술로 대체육과 생분해성 필름 개발이 주목받고 있다. 대체육은 최근 탄소배출로 인한 이상기후 현상을 회복하기 위해 축산의 최소화와 그로 인한 육제품 수요를 대체할 대체식품에 관심이 많아지고 있다. 대표적인 대체육 식품으로는 곤충육, 식물성 단백질, 배양육 등이 있다. 곤충육과 식물성 단백질은 자체적인 기호성이 낮기 때문에 분말화 하여 가식성 소재와 섞은 후 3D 바이오 프린터로 고기의 형태로 출력하는 방법으로 활용하고 있다 (그림 6).
그림 6. 곤충단백질식품을 출력하는 3D 바이오 프린터 [12].
가식성 소재에는 실제 고기의 맛을 구현하기 위한 향과 맛을 첨가하여 구성성분은 곤충육이나 식물성 단백질이지만 맛은 육고기의 맛을 내는 기술에 중점을 두고 있다. 추가적으로 곤충육과 식물성 단백질 외 육고기를 생산하는 방법, 축산이 아닌 배양기술을 이용한 배양육에 대한 관심이 높아지고 있다. 배양육은 가축의 줄기세포 혹은 근섬유세포를 채취하여 바이오 잉크와 섞어 출력 후, 배양액을 담은 배양기에서 조직이 될 때까지 배양한다 (그림 7). 3D 바이오 프린터를 이용하지 않고 배양할 경우, 고기의 형태가 아닌 부유물의 형태로 배양되기 때문에 3D 바이오 프린팅 지지층의 사용이 필연적이다. 본 기술은 미래식량의 핵심 기술이며, 4차 산업시대의 식품분야에서 필수적인 기술로 자리 잡을 것으로 사료된다.
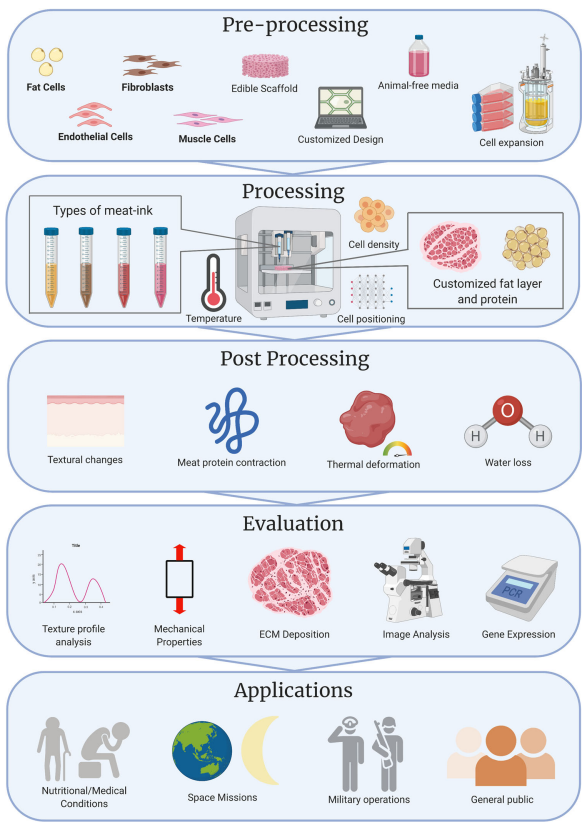
그림 7. 3D 바이오 프린터를 활용한 배양육 모식도 [13].
생분해성 플라스틱은 환경적 이슈에 가장 큰 문제 해결법 중 하나일 것이다. 플라스틱의 개발은 많은 영역에서 도약적 발전의 기초가 되었지만, 폐기된 플라스틱은 미세플라스틱으로 생물의 체내 침투, 바다생물의 플라스틱에 의한 문제 등 환경문제는 더욱 심각해지고 있다. 연구자들은 이러한 플라스틱의 문제를 해결하기 위해 천연 유래의 생분해성 물질을 활용한 플라스틱 대체 연구에 전력을 다하고 있다. 대표적으로 poly(lactic) acid, agar, sodium carboxymethylcellulose, gelatin, alginate, cellulose nanofiber, collagen 등이 있다. 생분해성 플라스틱의 생산과정에서 가장 큰 한계점은 낮은 녹는점에 의한 기존 플라스틱 생산 공법을 사용하지 못한다는 점이다. Solution casting 방법으로 용매에 녹여 건조시켜 만드는 방법이 가장 일반적이지만, 이 방법은 Scale-up 단계에서 경계성이 확보되지 않는다. 또한 일정한 품질관리를 위해 더욱 섬세한 제조 방법이 도입되어야한다. 이러한 문제점을 해결할 방법으로 3D 바이오 프린터의 기술에 주목하고 있다. 3D 바이오 프린터는 3D 프린터와 달리 열을 사용하지 않고 공기의 압출에 의한 출력방식으로 생분해성 소재를 원하는 두께와 모양으로 출력할 수 있다. 단순히 포장 필름뿐만 아니라, 포장 용기, 빨대 등 다양한 모양으로 출력하여 생분해성 플라스틱의 활용도가 더욱 높아질 것으로 사료된다.
참고문헌
[1] N.A. Charoo, S.F. Barakh Ali, E.M. Mohamed, M.A. Kuttolamadom, T. Ozkan, M.A. Khan, et al., Selective laser sintering
3D printing–an overview of the technology and pharmaceutical applications, Drug Dev. Ind. Pharm. 46 (2020) 869-877.
[2] M.P. Lee, G.J. Cooper, T. Hinkley, G.M. Gibson, M.J. Padgett, L. Cronin, Development of a 3D printer using scanning
projection stereolithography, Scientific reports. 5 (2015) 1-5.
[3] S.S. Crump, The fused deposition modeling (FDM), United States Patent Applications. 5,121,329 and 5,340,433 (1988).
[4] N.T. Aboulkhair, M. Simonelli, L. Parry, I. Ashcroft, C. Tuck, R. Hague, 3D printing of Aluminium alloys: Additive
Manufacturing of Aluminium alloys using selective laser melting, Progress in materials science. 106 (2019) 100578.
[5] F.A. Shah, O. Omar, F. Suska, A. Snis, A. Matic, L. Emanuelsson, et al., Long-term osseointegration of 3D printed CoCr
constructs with an interconnected open-pore architecture prepared by electron beam melting, Acta biomaterialia. 36 (2016) 296-309.
[6] Q. Ramadan, M. Zourob, 3D bioprinting at the frontier of regenerative medicine, pharmaceutical, and food industries,
 JOIN
JOIN LOGIN
LOGIN
 Latest update
Latest update