| 3차원 나노/마이크로 구조를 활용한 줄기세포 분화 응용기술 | |
|---|---|
| Date 2022-04-09 16:45:04 |
|

선임연구원
한국과학기술연구원 (KIST) 뇌과학연구소
h.seong@kist.re.kr
1. 서론
줄기세포(stem cell)는 자가복제능력을 가지고 있으며, 우리 몸을 구성하는 다양한 조직세포로 분화할 수 있는 만능세포를 뜻한다. 이에 줄기세포는 노화, 질병, 부상 등으로 손상된 조직과 장기의 기능을 회복하기 위한 치료제로서 많은 주목을 받고 있다 [1,2]. 그러나 줄기세포가 실제 임상에서 활용되기 위해서는 극복해야 할 문제점들이 많다. 이는 줄기세포의 증식 및 배양이 까다로우며, 세포의 분화 정도를 정밀하게 조절하는 것이 어렵기 때문이다. 이러한 문제점들을 해결하기 위해, 많은 연구자들이 줄기세포의 분화를 보다 정밀하게 조절하기 위한 방법들을 연구하고 있다.
줄기세포는 생체 내의 주변 환경을 이루는 세포외 기질 (extracellular matrix, ECM)의 화학적 또는 물리적 특성에 영향을 받기 때문에, 3차원의 나노/마이크로 구조를 배양 플랫폼으로 활용하면 줄기세포의 분화와 성장을 조절할 수 있게 된다 [3,4]. 본 기고문에서는 다양한 3차원의 나노/마이크로 구조체를 구현하기 위한 방법에 대해 설명하고, 각 방법으로 구현된 다양한 구조체들이 줄기세포의 배양 및 분화에 어떻게 활용되고 있는지 살펴보고자 한다.
2. 본론
2.1. 포토리소그래피 (photolithography)와 전자빔 리소그래피 (e-beam lithography)를 이용한 나노패턴 제작과 응용
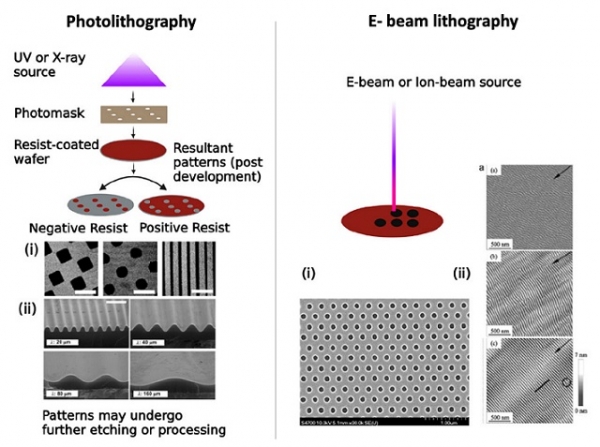
리소그래피 기술은 반도체 공정에서 미세 패턴을 제작하기 위해 사용되는데, 그 중 표면에 감광성 고분자를 도포하고 자외선 (UV) 광원을 사용하여 마스크에 그려진 패턴을 전사하는 포토리소그래피가 가장 널리 쓰이는 방법이다 (그림 1). 마스크의 디자인이 용이하고 빠른 시간에 넓은 면적의 패터닝을 진행할 수 있다는 장점을 가진다.
그림 1. Photolithography와 e-beam lithography의 모식도 (J. Carthew et al., ACS Appl. Mater. Interfaces, 2022).
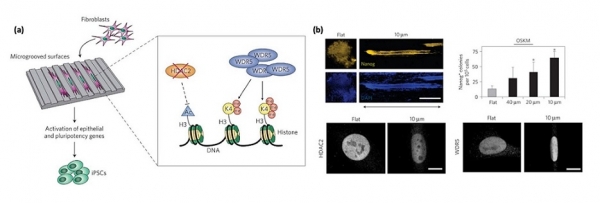
포토리소그래피를 활용하여 가장 많이 연구된 패턴 중 하나는 마이크로 격자구조(microgroove)인데, 주로 5~50 μm 가량의 선폭 및 높이를 가진다. 격자구조 위에 세포를 배양하게 되면 격자 사이사이에 세포가 배열되어 격자 형태를 따라 자라게 되며, 이로 인해 세포의 골격 (cytoskelecton)과 초점접착 (focal adhesion, FA)이 변형된다. 이로 인해 세포 내 분화능도 영향을 받는 것으로 알려져 있다 (그림 2) [5]. 이를 활용하여 표피세포, 골세포, 줄기세포 등 다양한 세포를 패턴 위에 배양하였을 때 세포의 분화능에 어떤 영향을 미치는지에 대해 활발히 연구되고 있다.
그림 2. (a) 폭 10 μm, 높이 3 μm의 PDMS 재질 마이크로 격자구조를 이용한 mouse fibroblast의 iPSC로의 분화 유도 모식도 (Y. Xu et al., Nat. Mater. 2013). (b) 격자구조가 조밀해질수록, 세포의 분화능 유지 정도를 판단하는 발현인자 중 하나인 Nanog-positive 세포가 더 많이 발현된다. 이에 대한 기작으로서 마이크로 격자구조가 HDAC를 억제시키고, WDR5를 촉진시켜 이러한 분화 유도를 야기하는 이론을 제시하였다. (T. L. Downinge t al., Nat. Mater. 2013).
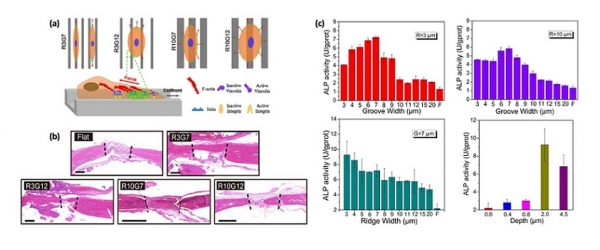
특히 이러한 세포 거동 변화에 착안하여, 임플란트와 같은 이식용 생체재료의 표면에 마이크로 격자구조를 식각하여 임플란트의 이식 후 주변 조직과의 융화를 촉진시키는 연구도 활발히 진행되고 있다. 2019년 중국의 연구진들이 발표한 논문이 흥미로운데, 이 연구진들은 인공뼈 구조물로 널리 활용되는 티타늄 (titanium, Ti)에 다양한 길이의 마이크로 격자구조를 패터닝하여 동물 모델에 삽입하였다 [6]. 이를 통해 조골세포 (osteoblast)를 분화시켰을 때 골세포로 분화되는 정도에 차이가 있음을 관찰하였는데, 이 결과가 동물 모델 내에서도 유사한 결과를 보임을 확인하였다.
그림 3. (a) Ti를 재료로 한 다양한 길이의 마이크로 격자구조 위에서 자란 MC3T3-E1 osteoblasts의 focal adhesion (FA) 염색결과 및 (b) 마이크로 격자구조가 조밀해짐에 따라 세포의 형태 및 FA가 변화하는 메커니즘 모식도. (c) 마이크로 격자구조가 형성된 Ti 디스크를 동물 두개골에 이식한 후, 8주 뒤 조직염색한 결과. 조밀한 구조를 가지는 마이크로 격자구조가 두개골과 더 잘 융화됨을 확인할 수 있다 (Zhu et al., ACS Appl. Mater. Interfaces 2019).
그러나 세포의 FA 형성이 나노 크기로 이루어지는 점을 감안하였을 때, 줄기세포를 보다 정밀하게 조절하기 위해서는 2 μm 미만의 나노구조를 구현할 필요가 있다. 이는 포토리소그래피 기술로는 구현하기 어려운데, 이를 극복하기 위해 활용되는 방법 중 하나는 마스크 없이 전자빔 등의 광원을 선택적으로 조사하여 패턴을 형성하는 직접 기록 리소그래피 공정이다.
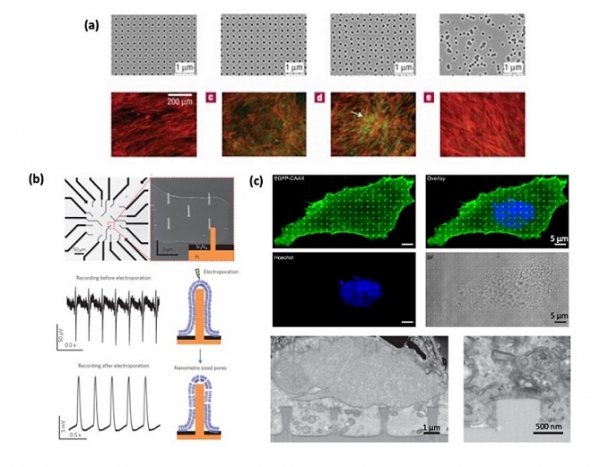
전자빔 리소그래피를 활용하여 가장 활발히 연구된 구조는, 볼록한 형태의 나노기둥 (nanopillar) 또는 반대 형태의 나노구멍 (nanohole)이다. 2007년 Nat. Mater.에 소개된 연구결과가 대표적인데 (그림 4(a)), 200 nm 지름을 가지는 나노구멍의 배열이 규칙적일 때와 불규칙할 때의 골수유래 줄기세포 분화능을 비교한 결과 약간의 불규칙성을 가진 배열에서 골세포로의 분화능력이 극대화됨을 확인하였다 [7].
또한 전자빔 리소그래피의 고정밀성을 활용하여, 세포 내 전기적 신호를 측정하기 위한 나노전극을 만드는 연구도 주목을 받고 있다 (그림 4(b)). Stanford University의 Bianxiao Cui 연구그룹은 전통적으로 사용되던 2차원 microelectrode array (MEA)에 나노기둥 구조를 병합시켜, 3차원 나노기둥 구조를 활용하였을 때 보다 정밀한 세포신호를 측정할 수 있음을 보였다 [8,9]. 이는 세포막이 나노기둥을 둘러싸면서, 나노기둥이 세포 내부까지 깊숙이 침투할 수 있었기 때문이다. 작은 전극 패드 하나하나에 패터닝을 할 수 있을 만큼 전자빔 리소그래피는 현존하는 나노공정 기술 중 가장 높은 정밀도를 가지지만, 공정비용이 비싸고 대면적 표면을 처리하기에는 적절하지 못하다는 단점을 가진다.
그림 4. (a) 전자빔 리소그래피를 이용해 제작된 200 nm 크기 나노구멍의 배열 변화에 따른 골수줄기세포 분화 양상 차이. 붉은색: Actin, 녹색: Osteocalcein (M. J. Dalby et al., Nat. Mater. 2007). (b) 전극패드 위에 제작된 지름 100 nm의 나노기둥 및 이를 통한 세포 내 전위 측정 (L. Hanson et al., Nat. Nanotech. 2015). (c) 정렬된 나노기둥과 세포의 접착을 관찰하기 위한 형광 사진 및 단면 SEM 사진 (X. Li eat l., Nat. Protocol, 2019).
2.2. 나노임프린트 리소그래피 (Nanoimprint lithography, NIL)를 이용한 나노패턴 제작과 응용
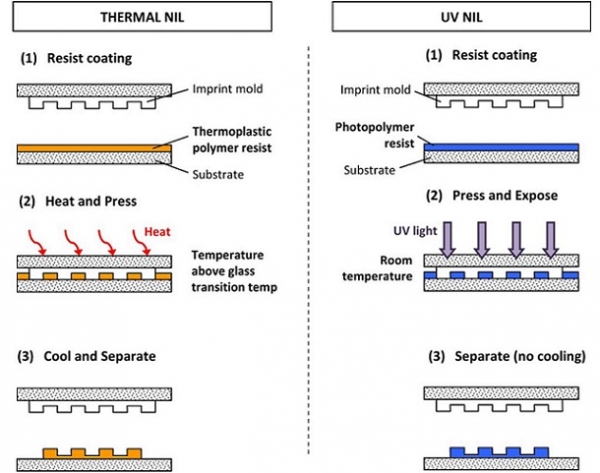
NIL은 유동성을 가진 얇은 고분자층에 포토리소그래피 또는 전자빔 리소그래피를 통해 제작한 주형 (master mold)을 접촉시켜 물리적으로 눌러내어 고분자 층을 패터닝하는 공정을 통칭한다. 사용되는 고분자는 열에 변형되거나, 자외선 등의 빛에 경화되는 특성을 가지며 열에 변형되는 고분자를 활용하는 경우 thermal NIL, 자외선에 경화되는 고분자를 활용하는 경우 UV NIL로 나누어 구분한다 (그림 5).
NIL 기술은 주형으로부터 패턴을 반복하여 얻을 수 있기 때문에, 기존의 패턴 제작 기술에 비해 제작 단가가 낮고 공정 시간이 짧다는 장점을 가진다 [10]. 특히 NIL을 통해 제작된 나노/마이크로 패턴들은 고분자 물질을 기반으로 하기 때문에, 금속이나 실리콘과 같은 디바이스 제작에 쓰이는 재료에 비해 세포독성 (cell cytotoxicity)이 낮고 생체적합성 (biocompatibility)이 우수하다는 장점이 있어, 세포 배양 분야에 활용되기에 적합성이 높다.
그림 5. Thermal NIL과 UV NIL의 공정 모식도 (N. Kooy et al., Nanoscale Res. Lett. 2014).
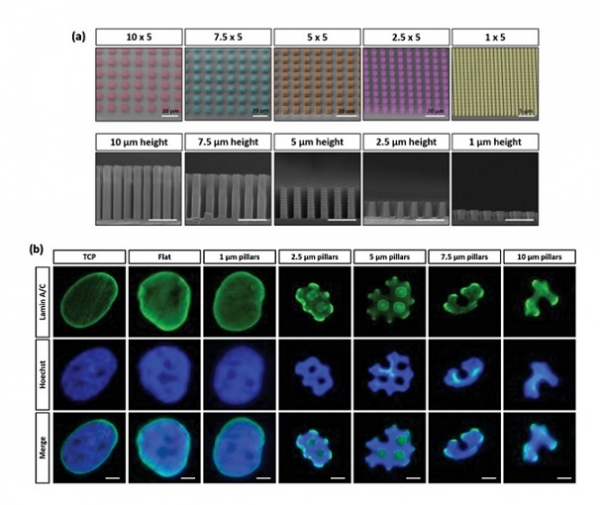
이러한 장점을 활용하여 선형 패턴, 기둥패턴, 원뿔 패턴 등 다양한 형태의 패턴들이 제작되어 세포 배양에 활용되고 있다. 2021 년 Advanced Science에 발표된 연구결과의 경우, OrmoComp라는 광경화성 유-무기 복합 고분자를 활용하여 1~10 μm 높이를 가지는 마이크로 기둥을 제작하였는데 마이크로 기둥의 높이에 따라 세포의 핵 (nuclear) 구조 변형 정도가 크게 달라짐을 보인 점이 흥미롭다 [11]. 핵 구조의 변형은 핵막 (nuclear membrane) 주변부와 연결된 유전자 변형에 기여하는 단백질에도 영향을 주어, 줄기세포의 분화에 간접적으로 기여하게 된다. 이렇게 세포에 가해진 물리적 자극이 세포 반응으로 전환되는 것을 역학전이 (mechanotransduction)라 하며, 이를 활용하여 줄기세포 분화를 보다 정밀하게 조절하는 연구가 활발히 진행되고 있다 [12].
그림 6. (a) UV NIL을 이용해 제작된 다양한 높이의 마이크로 기둥 및 (b) 기둥 높이 변화에 따른 핵막단백질 (Lamin A/C)과 핵 구조 변형 양상 (J. Cartew et al., Adv. Sci. 2021).
2.3. 실리콘 기반 고종횡비 (high-aspect-ratio) 패턴 제작과 응용
동일한 간격의 나노/마이크로 패턴이라 하더라도 높이 변화에 따라 역학전이가 일어나는 정도는 크게 달라진다. 이를 극대화하기 위해, 포토리소그래피를 이용하여 원하는 패턴을 만든 후 식각공정 (etching process)을 추가하는 top-down 공정이나 나노선 (nanowire)을 합성하는 bottom-up 공정을 이용하여 보다 높이가 높고 가느다란 형태의 구조를 만들기도 한다. 이를 통해 하부지름과 높이의 비율이 1:10 이상의 고종횡비 구조체들을 구현할 수 있게 된다 [13].
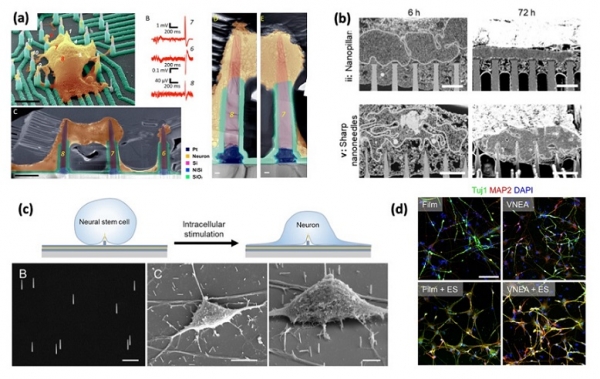
고종횡비 구조가 가지는 큰 장점 중 하나는, 구조가 세포에 보다 깊게 침투되도록 할 수 있다는 점이다. 이를 통해 세포 내부 신호를 읽는 전극으로서 활용하거나, 세포에 물리적인 자극을 줄 수 있다. 2017년 Nano Letters에 발표된 논문에서는 뉴런 하나에 2~3개의 식각공정을 통해 제작한 실리콘 3차원 마이크로 전극을 맞닿게 하여 뉴런 내부 전기신호를 읽을 수 있는 MEA를 개발하였다 (그림 7(a)) [14]. 2020년 ACS Nano에서는, 세포 내부에 보다 더 깊숙하게 침투할 수 있는 바늘 구조의 3차원 패턴을 구현하여, 구조의 미세한 변화에 따라 골수줄기세포의 분화능과 유전자 발현이 조절됨을 선보였다 (그림 7(b)) [15].
더 나아가, 고종횡비 패턴을 이용하게 되면 세포 내부에 물리적으로 자극을 가하거나 분화에 필요한 물질을 효율적으로 전달할 수도 있게 된다. 2021년 Nano Letters에 발표된 논문에서는 bottom-up 공정을 이용해 제작한 실리콘 나노선을 활용하여 신경줄기세포 (neural stem cell) 내부에 전기자극을 주었을 때 뉴런으로의 분화능이 향상됨을 선보인 바 있다 (그림 7 (c, d)) [16]. 뉴런이 상호간의 전기적 신호 교류로 작동하는 세포임을 감안하였을 때, 신경줄기세포로부터 분화된 뉴런이 보다 더 정밀하게 동작할 수 있게끔 하는 방법으로서 활용될 수 있어 매우 흥미롭다.
그림 7. (a) 7 μm 높이 실리콘 전극. 세포 내 전기신호를 읽는 전극으로서 활용되었다 (R. Liu et al., Nano Lett. 2017). (b) 2 μm 간격의 나노기둥 구조 (head size: 700 nm)와 나노바늘 구조 (head size: < 20 nm)가 세포 배양에 활용되었을 때의 세포-구조 접촉 단면 (H. Seong et al., ACS Nano 2020). 나노바늘 구조를 사용하였을 때 세포에 보다 깊이 침투할 수 있음을 확인할 수 있다. (c, d) Bottom-up approach를 이용해 제작된 실리콘 나노와이어를 활용한 neural stem cell 전기자극 모식도 및 분화 이후 세포염색 결과 (J. Kwon et al., Nano Lett. 2021).
3. 결론 및 전망
줄기세포 배양 및 분화기술은 그간 약물로 치료가 어려웠던 파킨슨병, 신경퇴화 등의 여러 가지 퇴행성 질환들을 치료할 수 있는 꿈의 치료법이 될 수 있어, 재생의료 분야에서 많은 주목을 받고 있다.
나노패턴 구조의 변화가 어떠한 원리로 줄기세포에 영향을 주는지에 대한 메커니즘은 현재까지도 정확히 밝혀져 있지 않으나, 나노 가공 기술의 발전에 힘입어 줄기세포별 맞춤형 나노패턴을 제작하는 등 연구의 성숙도가 높아지고 있다. 특히 본 기고문에서 다룬 3차원 구조들은 줄기세포 내부의 전기적/화학적 신호를 읽는 관찰 플랫폼을 제작하는 융합 연구에도 쓰일 수 있다 [17]. 향후에는 3차원 구조들이 단순히 줄기세포의 분화를 촉진하는 외부 자극 요인으로서만 사용되는 것이 아니라, 줄기세포의 전기화학적 거동을 보다 정확하게 분석하고, 생체 시스템을 이해하는 데 활용될 수 있을 것으로 기대한다.
참고문헌
1. S. W. Lane, D. A. William, F. M. Watt, Modulating the stem cell niche for tissue regeneration, Nat. Biotech. 2014, 21, 795-803
2. C. S. Chen, M. Mrksich, S. Huang, G. M. Whitesides, D. E. Ingber, Geometric control of cell life and death, Science, 1997, 276, 1425-1428
3. T. C. von Erlack, S. Bertazzo, M. A. Wozniak, C.-M. Horejs, S. A. Maynard, S. Attwood, B. K. Robinson, H. Autefage, C. Kallepitis, A. D. R. Hernandex, C. S. Chen, S. Goldoni, M. M. Stevens, Cell-geometry-dependent changes in plasma membrane order direct stem signalling and fate, Nat. Mater. 2018, 17, 237-242
4. E. K. Yim, E. M. Darling, K. Kulangara, F. Guilak, K. W. Leong, Nanotopography-induced changes in focal adhesions, cytoskeletal organization, and mechanical properties of human mesenchymal stem cells. Biomaterials, 2010, 31, 1299–1306
5. T. L. Downing, J. Soto, C. Morez, T. Houssin, A. Fritz, F. Yuan, J. Chu, S. Patel, D. V. Schaffer, S. Li, Biophysical regulation of epigenetic state and cell reprogramming, Nat. Mater. 2013, 12, 1154-1162
6. M. Zhu, H. Ye, J. Fang, C. Zhong, J. Yao, J. Park, X. Lu, F. Ren, Engineering high-resolution micropatterns directly onto titanium with optimized contact guidance to promote osteogenic differentiation and bone regeneration, ACS Appl. Mater. Interfaces 2019, 11, 43888-43901
7. R. J. McMurray, N. Gadegaard, P. M. Tsimbouri, K. V. Burgess, L. E. McNamara, R. Tare, K. Murawaski, E. Kingham, R. O. C. Oreffo, M. J. Dalby, Nanoscale surfaces for the long-term maintenance of mesenchymal stem cell phenotype and multipotency, Nat. Mater. 2011, 10, 637–644 (2011).
8. L. Hanson, W. Zhao, H.-Y. Lou, Z. C. Lin, S. W. Lee, P. Chowdry, Y. Cui, B. Cui, Vertical nanopillars for in situ probing of nuclear mechanics in adherent cells, Nat. Nanotech. 2015, 10, 554-562
9. X. Li, L. Matino, W. Zhang, L. Klausen, A. F McGuire, C. Lubrano, W. Zhao, F. Santoro, B. Cu, A nanostructure platform for live-cell manipulation of membrane curvature, Nat. Protocol, 2019, 14,6,1772-1802
10. N. Kooy, K. Mohamed, L. T. Pin, O. S. Guan, A review of roll-to-roll nanoimprint lithography, Nanoscale Res. Lett. 2014, 9, 320
11. J. Carthew, H. H. Abdelmaksoud, M. Hodgson-Garms, S. Aslanoglou, S. Ghavamian, R. Elnathan, J. P. Spatz, J. Brugger, H. Thissen, N. H. Voelcker, V. J. Cadarso, J. E. Frith, Precision Surface Microtoography Regulates Cell Fate via Changes to Actomyosin Contractility and Nuclear Architecture, Adv. Sci. 2021, 8, 2003186
12. P. Romani, L. Valcarcel-Jimenez, C. Frezza, S. Dupont, Crosstalk between mechanotransduction and metabolism, Nat. Rev. Mol. Cell Bio. 22, 22-38 (2021)
13. S. G. Higgins, M. Becce, A. Belessiotis-Richard, H. Seong, J. E. Sero, M. M. Stevens, High-Aspect-Ratio Nanostructured Surfaces as Biological Metamaterials, Adv. Mater. 32, 1903862
14. R. Liu, R. Chen, A. T. Elthakeb, S. H. Lee, S. Hinckley, M. L. Khraiche, J. Scott, D. Pre, Y. Hwang, A. Tanaka, Y. G. Ro, A. K. Matsushita, X. Dai, C. Soci, S. Biesmans, A. James, J. Nogan, K. L. Jungjohann, D. V. Pete, D. B. Webb, Y. Zou, A. G. Bang, S. A. Dayeh, High Density Individually Addressable Nanowire Arrays RecordIntracellular Activity from Primary Rodent and Human Stem Cell Derived Neurons, Nano Lett. 2017, 17, 2757-2764
15. H. Seong, S. G Higgins, J. Penders, J. P. K. Armstrong, S. W. Crowder, A. C. Moore, J. E. Sero, M. Becce, M. M. Stevens, Sizetunable nanoneedle arrays for influencing stem cell morphology, gene expression, and nuclear membrane curvature, ACS Nano 2020, 14, 5371-5381
16. J. Kwon, J. S. Lee, J. Lee, J. Na, J. Sung, H.-J. Lee, H. Kwak, E. Cheong, S.-W. Cho, H.-J. Choi, Vertical Nanowire Electrode Array for Enhanced Neurogenesis of Human Neural Stem Cells via Intracellular Electrical Stimulation, Nano Lett. 2021, 21, 6343-6351
17. R. Liu, J. Lee, Y. Tchoe, D. Pre, A. W. Bourhis, A. D’Antonio-Chronowska, G. Robin, S. H. Lee, Y. G. Ro, R. Vatsyayan, K. J. Tonsfeldt, L. A. Hossain, M. L. Phipps, J. Yoo, J. Nogan, J. S. Martinez, K. A. Frazer, A. G. Bang, S. A. Dayeh, Ultra-sharp nanowire arrays natively permeate, record, and stimulate intracellular activity in neuronal and cardiac networks, Adv. Funct. Mater. 2021, 2108378
 JOIN
JOIN LOGIN
LOGIN
 Latest update
Latest update